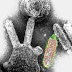
חיידק טורף שהוסף למזונן של תרנגולות הקטין את כמות חיידקי הסלמונלה במעיהן
 |
חיידקי Salmonella typhimurium (באדום) צמודים לתאי אדם בתרבית. |
לפני כשלוש שנים, כתבתי על חיידקי ה-Bdellovibrio bacteriovorus, חיידקים קטנים הטורפים חיידקים גדולים מהם. במדור הועלתה האפשרות שבתום העידן האנטיביוטי נוכל להשתמש בהם כאמצעי כנגד חיידקים גורמי מחלות. כאן אדווח על שימוש ראשון בחיידקים הטורפים בבעלי חיים חמי דם, לאחר שכל הניסויים הקודמים נעשו בצמחים, בדו-חיים ובדגים.
חיידקי Bdellovibrio ביחד עם טרף פוטנציאלי, חיידקי Escherichia coli.
By kind permission George A. O'Toole, Dept. of Microbiology & Immunology,
Dartmouth Medical School, Hanover
קבוצת חוקרים מאוניברסיטת נוטינגהם, בראשות פרופ' ליז סוקט (Sockett), החליטה לבדוק את השפעת זן של חיידקי B. bacteriovorus, שטורף חיידקי סלמונלה במבחנה, על חיידקי סלמונלה במעיים של תרנגולות חיות. בניסוי מקדים, שנועד לבדוק את הבטיחות שבשימוש בחיידקים הטורפים, הוסיפו החוקרים למזונם של 12 אפרוחים את החיידקים הטורפים, והשוו את גידולם והתפתחותם במשך 28 ימים לקבוצת אפרוחים מקבילה שלמזונה הוסף רק הנוזל שבו הורחפו החיידקים (בלי החיידקים). לא היה כל הבדל בהתפתחות ובגדילה של שתי קבוצות האפרוחים, כך שהוכח שהחיידקים בטוחים לשימוש.הניסוי העיקרי, שנועד לבדוק את היכולת המניעתית/טיפולית של החיידקים הטורפים, כלל שלוש קבוצות של 18 תרנגולות, שלמזונן הוספו - 10 ימים לפני הניסוי - חיידקי סלמונלה מזן המוכר כמחולל מחלה (בבני אדם) בארצות אירופה בשלושת העשורים האחרונים . למזון של קבוצת הניסוי הוספו חיידקי B. bacteriovorus, עם נוגד חומצה (כדי שישרדו את המעבר בקיבה), ואילו למזון של קבוצת הביקורת הראשונה הוספו חיידקים מוטנטיים של B. bacteriovorus, חסרי יכולת הטריפה, באותם תנאים. לקבוצת הביקורת השנייה הוספו רק נוגד החומצה והנוזל שבו הורחפו החיידקים. במהלך שלושה ימים נערכה ספירה של חיידקי סלמונלה ובדקו את השינויים בתכולת חיידקי הסלמונלה במעיים של התרנגולות לאורך זמן. רק בנוכחות החיידקים הטורפים - בקבוצת הניסוי, היתה ירידה משמעותית בכמות חיידקי הסלמונלה, יחסית לשתי קבוצות הביקורת.
הצלחת הניסוי תאפשר להשתמש בחיידקים הטורפים בהפחתת חיידקי הסלמונלה הפתוגניים בבעלי חיים. בהמשך תיבדק האפשרות לטפל בבני אדם באמצעות משחה או תרחיף המכילים חיידקי B. bacteriovorus בפצעים חיצוניים שזוהמו על ידי חיידקים (בעיקר Pseudomonas), ואולי גם בזיהומים מערכתיים הנגרמים על-ידי חיידקים אחרים הרגישים לחיידקים הטורפים.
לקריאה נוספת
המאמר המקורי:
R. J. Atterbury, L. Hobley, R. Till, C. Lambert, M. J. Capeness, T. R. Lerner, A. K. Fenton, P. Barrow, R. E. Sockett. Studying the effects of orally administered Bdellovibrio on the wellbeing and Salmonella colonization of young chicks. Applied and Environmental Microbiology, 2011;
דרור בר-ניר, "חיידקים טורפי חיידקים", "גליליאו" 114, (2008);
פורסם במקור ב"גליליאו" גיליון 157, עמוד 13, ספטמבר 2011.