אחד המאפיינים הביוכימיים של החיידקים, המקנה להם יציבות בתנאים היפוטוניים (כשריכוז המומסים מחוץ לתא נמוך מהריכוז בתוך התא), הוא הפולימר פפטידוגליקן (peptidoglycan), המרכיב העיקרי של הדופן. בתנאים היפוטוניים חודרים (באוסמוזה) מים לתוך התא ואלמלא הדופן, היו החיידקים מתפוצצים. הפפטידוגליקן מורכב מיחידות חוזרות (מונומרים) הבנויות מדו-סוכר אליו קשור פנטה-פפטיד (פפטיד בן חמש חומצות אמיניות). המונומרים מיוצרים בתוך התא החיידקי, מופרשים החוצה - הסוכרים מצורפים לשרשרת הסוכרים על-ידי האנזים transglycosylase, ולאחריו האנזים transpeptidase יוצר קשרי צילוב בין השייר הרביעי בפפטיד של מונומר אחד, לשייר השלישי של מונומר אחר. במהלך התהליך נפלטת מהמונומר החומצה האמינית החמישית, והאנרגיה המשתחרת מהקשר שנפתח מושקעת בקשר הצילוב. הקשר יכול להיות ישיר (כמו בחיידקים מחטיבת הפרוטאובקטריה) או דרך גשר של גליצינים (למשל ב-Staphylococci, מחטיבת הפירמיקוטים). שלב הטרנספפטידציה תורם לחוזקה של הדופן ועמידותה בפני לחצים אוסמוטיים, ובלעדיו הדופן פגומה ואינה מתפקדת - ואז חודרים מים לתאי החיידקים והם מתנפחים ומתפוצצים.
 |
| היחידה המבנית של הפפטידוגליקן בחיידקים מהפירמיקוטים. המקור |
קיימות שתי קבוצות של תרופות הקוטלות חיידקים על ידי פגיעה בשלב זה. התרופות מהקבוצה הראשונה, הכוללת, בין היתר, את האנטיביוטים פניצילינים (ראו "סֵר אלכסנדר פלמינג - מגלה הפניצילין") וצפלוספירינים, נצמדות לאתר הפעיל של האנזים transpeptidase ובכך מנטרלות את פעילותו. אנטיביוטים אחרים, כגליקופפטידים ונקומיצין (vancomycin) ואוופרסין (avoparcin), נקשרים לאתר המטרה של האנזים, הקצה של הפנטפפטיד - הדי-פפטיד D-ala-D-ala, ובכך חוסמות את הגישה של האנזים לאתר. חשוב לציין שאנטיביוטים אלה פוגעים אך ורק בתאים גדלים ומתחלקים - אז מתקיימת סינתזה פעילה של דופן. תאים שאינם מתחלקים ולא מתרחשת בהם סינתזת דופן - אינם מושפעים מהאנטיביוטים. כמובן שחיידקים חסרי פפטידוגליקן, כ-Mycoplasma (שהם חסרי דופן בכלל) ו-Planctomyces (שם הדופן אינה מורכבת מפפטידוגליקן), עמידים באופן טבעי בפניהם.
במשך הזמן חיידקים גורמי מחלות, וביניהם Enterococci ו-Staphylococci, פיתחו או רכשו מנגנוני עמידות כלפי האנטיביוטים האלה (והאחרים) כך שאנו מתקרבים למצב שבו האנטיביוטים לא יהיו שמישים במאבק בהם (ראו גם ב"פרדוקס בתי-החולים וסוף עידן האנטיביוטיקה").
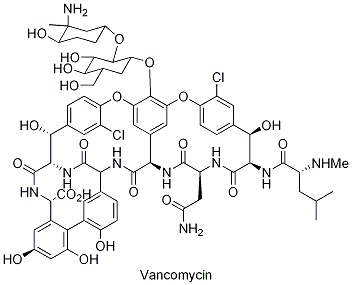
הגליקופפטיד ונקומיצין התגלה לראשונה בשנות החמישים של המאה הקודמת על-ידי אדמונד קורנפלד (Kornfeld) מחברת Eli Lilly. החיידק שממנו הופרש האנטיביוט, מקבוצת האקטינובקטריה, שהיום מכונה Amycolatopsis orientalis, בודד מדגימת אדמה שנשלחה לחברה ב-1953 מיערות בורניאו. הוונקומיצין, שאז כונה תרכובת 05865, אושר לשימוש על-ידי ה-FDA בשנת 1958.
ונקומיצין מסונתז במספר שלבים ממספר חומצות אמיניות בתא החיידקי. הוא מופק מהחיידקים.
הונקומיצין נחשב, מ-1958 עד לפני כשני עשורים, כאנטיביוט המנצח של המוצא האחרון (ומכאן גם שמו - vanquish = להביס, לנצח), לטיפול בזיהומים חמורים הנובעים בעיקר מ-Staphylococcus aureus עמיד לפניצילינים (MRSA).
עקב גודלו ותכונותיו, הוא אינו חודר את הממברנה החיצונית של חיידקים מהפרוטאובקטריה, ואינו חודר ממערכת העיכול לדם, השימוש בו היה בהזרקה ישירה לדם בלבד. ניתן להשתמש בונקומיצין דרך הפה בזיהומים חמורים במערכת העיכול, למשל על ידי Clostridium difficile, הגורם ל-Pseudomembranous colitis (אם כי לפעמים גם הוא לא עוזר. ראו "חיידקי מעיים - להצלת חיים").
לוונקומיצין פותחו מספר נגזרות, oritavancin ו-dalbavancin. לנגזרות אלה זמן מחצית חיים ארוך יותר המאפשר מרווח גדול בין ההזרקות. אנטיביוטים בעלי פעילות דומה לוונקומיצין הם teicoplanin, שבודד בתחילת שנות ה-90 של המאה הקודמת מהחיידק Actinoplanes teichomyceticus ולו זמן מחצית חיים ארוך יותר וחדירות טובה יותר, ו-Ramoplanin שבודד ממין אחר של Actinoplanes.
בסוף שנות ה-90 של המאה הקודמת החלו להופיע ברחבי העולם חיידקים עמידים לוונקומיצין. בניגוד למקרים קודמים, בהם עמידויות ראשונות כלפי חומרים אנטיביוטים הופיעו תחילה בבתי חולים, העמידות לוונקומיצין התפתחה קודם בקהילה ובבדיקות מדוקדקות יותר התברר שהעמידות התפתחה במגזר החקלאי באירופה, באוסטרליה ובמקומות אחרים, שם השתמשו, החל מ-1970, באנטיביוט אוופרסין, אנטיביוט דמוי ונקומיצין, שבודד מהחיידק Streptomyces candidus, כתוסף מזון. ב-1997 נאסר לבסוף השימוש באוופרסין, אבל זה היה כבר מאוחר - העמידות התפשטה ברחבי העולם.
חיידקים עמידים לפניצילין מכילים, בדרך כלל, אנזימים המפרקים את האנטיביוט. לעומת זאת עמידות לוונקומיצין מושגת על ידי שינוי במבנה המונומר המרכיב את הפפטידוגליקן: ה-D-אלנין האחרון במונומר, בעמדה החמישית, מוחלף בחומצה אמינית אחרת או בחומצה לקטית. – כך משתנה אתר המטרה של הונקומיצין והוא אינו יכול להקשר אליו. השינוי אינו משפיע על פעילות הטרנספפטידז.
דייל בוגר (Boger) ועמיתיו ממכון המחקר Scripps שבקליפורניה חקרו לעומק את המבנה המולקולרי של הוונקומיצין ופיתחו שתי נגזרות פעילות של ונקומיצין. הנגזרת הראשונה, בה החלפת אטום חמצן אחד באתר הפעיל של הגליקופפטיד בקבוצה אמידית, NH, גרמה לכך שהנגזרת, המכונה vancomycin amidine, תעצור את סינתזת הדופן גם בחיידקים העמידים לוונקומיצין המוכרים. הנגזרת השנייה, לה הוסיפו בנוסף לשינוי של הנגזרת הראשונה גם שייר כימי גדול יחסית – Chlorobiphenil, ובקיצור CBP, באזור אחר של המולקולה, גורמת לכך שהמולקולה פועלת כנגד חיידקים במנגנון נוסף, שעוד לא ברור מהו, מלבד מניעת הטרנספפטידציה. (החוקרים משערים שמדובר בעיכוב של האנזים טרנסגליקוזילז – אך זה עדיין מצריך בדיקה.)
 |
| המבנה הכימי של הונקומיצין החדש - השינויים - בצבעים. המקור |
שימוש מושכל באנטיביוט החדש, לאחר שיאושר השימוש בו, יכול לדחות את קץ עידן האנטיביוטיקה בכמה שנים.
לקריאה נוספת
המאמר המקורי
סֵר אלכסנדר פלמינג - מגלה הפניצילין -
חיידקי מעיים להצלת חיים
פרדוקס בתי-החולים וסוף עידן האנטיביוטיקה

אין תגובות:
הוסף רשומת תגובה